De vuelta a los mamíferos para hablar hoy de un Artiodáctilo
La palabra artiodáctilo deriva del griego "ártios" que significa par y "dáktylos" que significa dedo. Así que sabiendo esto y parándose a pensar un poco ya nos damos cuenta que voy a hablar de algún ungulado.
Ya sabemos de cuando hablé por primera vez de una vaca que los artiodáctilos son un orden de mamíferos ungulados cuyas extremidades terminan en un número par de dedos de los cuales apoyan en el suelo por lo menos dos (normalmente tercero y cuarto que son los mas desarrollados). Habitan en todos los continentes, excepto en la Antártida. Incluyen alrededor de unas 235 especies repartidas en 10 familias.
Estos animales aparecieron por primera vez durante el inicio del Eoceno, hace unos 55 millones de años. En los Artiodactilos actuales el número de dedos es par excepto en los tayasuidos, cuyas patas posteriores tienen solo tres dedos funcionales. El eje de las patas pasa por esos dos dedos que se encuentran cubiertos de pezuñas y son el apoyo del animal. Los metacarpianos y metatarsianos de los dedos largos están fusionados formando lo que denominamos caña. El cúbito y el peroné están muy atrofiados mientras que el radio y la tibia tienen gran desarrollo. Muchos de estos animales tienen cuernos frontales cerca de las órbitas oculares que suelen estar recubiertos por piel o por una vaina de queratina. Existe atrofia de los incisivos superiores, los premolares no se encuentran premolarizados y los molares son grandes y con crestas longitudinales en una adaptación para triturar. Hay especies que tienen un estómago formado por una bolsa simple, pero los que son rumiantes tienen cuatro cámaras: rumen, redecilla, omaso y abomaso. Poseen glándulas olorosas en la cabeza, entre los dedos, en la región inguinal y, con menos frecuencia, alrededor del ano.
Los bóvidos (Familia Bovidae) son un grupo de Artiodáctilos que incluye a rumiantes estrictamente hervíboros como toros, antílopes,ovejas y cabras entre otros. En las etapas infantiles, los bóvidos solamente tienen desarrollado el abomaso y se alimentan únicamente de leche materna; en este momento no se los considera rumiantes. Aproximadamente a los tres meses de edad, según la especie, ya suelen tener en funcionamiento sus cuatro estómagos. En muchas especies tanto las hembras como los machos presentan cuernos huecos. La mayoría se congregan en grandes grupos con complejas estructuras sociales, anque los hay no gregarios. Los bóvidos cubren un extenso rango de climas y hábitats diferentes; pueden vivir en desiertos, tundra y en bosques tropicales.
La familia Bovidae está integrada por las siguientes subfamilias:
La palabra artiodáctilo deriva del griego "ártios" que significa par y "dáktylos" que significa dedo. Así que sabiendo esto y parándose a pensar un poco ya nos damos cuenta que voy a hablar de algún ungulado.
Ya sabemos de cuando hablé por primera vez de una vaca que los artiodáctilos son un orden de mamíferos ungulados cuyas extremidades terminan en un número par de dedos de los cuales apoyan en el suelo por lo menos dos (normalmente tercero y cuarto que son los mas desarrollados). Habitan en todos los continentes, excepto en la Antártida. Incluyen alrededor de unas 235 especies repartidas en 10 familias.
Estos animales aparecieron por primera vez durante el inicio del Eoceno, hace unos 55 millones de años. En los Artiodactilos actuales el número de dedos es par excepto en los tayasuidos, cuyas patas posteriores tienen solo tres dedos funcionales. El eje de las patas pasa por esos dos dedos que se encuentran cubiertos de pezuñas y son el apoyo del animal. Los metacarpianos y metatarsianos de los dedos largos están fusionados formando lo que denominamos caña. El cúbito y el peroné están muy atrofiados mientras que el radio y la tibia tienen gran desarrollo. Muchos de estos animales tienen cuernos frontales cerca de las órbitas oculares que suelen estar recubiertos por piel o por una vaina de queratina. Existe atrofia de los incisivos superiores, los premolares no se encuentran premolarizados y los molares son grandes y con crestas longitudinales en una adaptación para triturar. Hay especies que tienen un estómago formado por una bolsa simple, pero los que son rumiantes tienen cuatro cámaras: rumen, redecilla, omaso y abomaso. Poseen glándulas olorosas en la cabeza, entre los dedos, en la región inguinal y, con menos frecuencia, alrededor del ano.
Los bóvidos (Familia Bovidae) son un grupo de Artiodáctilos que incluye a rumiantes estrictamente hervíboros como toros, antílopes,ovejas y cabras entre otros. En las etapas infantiles, los bóvidos solamente tienen desarrollado el abomaso y se alimentan únicamente de leche materna; en este momento no se los considera rumiantes. Aproximadamente a los tres meses de edad, según la especie, ya suelen tener en funcionamiento sus cuatro estómagos. En muchas especies tanto las hembras como los machos presentan cuernos huecos. La mayoría se congregan en grandes grupos con complejas estructuras sociales, anque los hay no gregarios. Los bóvidos cubren un extenso rango de climas y hábitats diferentes; pueden vivir en desiertos, tundra y en bosques tropicales.
La familia Bovidae está integrada por las siguientes subfamilias:
- Subfamilia Aepycerotinae
- Subfamilia Alcelaphinae
- Subfamilia Antilopinae
- Subfamilia Bovinae
- Subfamilia Caprinae
- Subfamilia Cephalophinae
- Subfamilia Hippotraginae
- Subfamilia Reduncinae
Los caprinos se han clasificado tradicionalmente hasta hace poco de la siguiente manera:
- Ammotragus Blyth, 1840.
Ammotragus lervia (Pallas, 1777)
- Budorcas Hodgson, 1850.
Budorcas taxicolor Hodgson, 1850
- Capra Linnaeus, 1758
Capra aegagrus Erxleben, 1777
Capra caucasica Güldenstädt & Pallas, 17833?
Capra cylindricornis Blyth, 1841
Capra falconeri Wagner, 1839
Capra hircus Linnaeus, 1758 (sinónimo de Capra aegagrus hircus)
Capra ibex Linnaeus, 1758
Capra nubiana F. Cuvier, 1825
Capra pyrenaica Schinz, 1838
Capra sibirica Pallas, 1776
Capra walie Rüppell, 1835
Capra caucasica Güldenstädt & Pallas, 17833?
Capra cylindricornis Blyth, 1841
Capra falconeri Wagner, 1839
Capra hircus Linnaeus, 1758 (sinónimo de Capra aegagrus hircus)
Capra ibex Linnaeus, 1758
Capra nubiana F. Cuvier, 1825
Capra pyrenaica Schinz, 1838
Capra sibirica Pallas, 1776
Capra walie Rüppell, 1835
- Capricornis Ogilby, 1836
Capricornis crispus Temminck, 1836
Capricornis milneedwardsii David, 1869
Capricornis rubidus Blyth, 1863
Capricornis sumatraensis Bechstein, 1799
Capricornis swinhoei Gray, 1862
Capricornis thar Hodgson, 1831
Capricornis milneedwardsii David, 1869
Capricornis rubidus Blyth, 1863
Capricornis sumatraensis Bechstein, 1799
Capricornis swinhoei Gray, 1862
Capricornis thar Hodgson, 1831
- Hemitragus Hodgson, 1841
Hemitragus hylocrius Ogilby, 1838
Hemitragus jayakari Thomas, 1894
Hemitragus jemlahicus H. Smith, 1826
Hemitragus jayakari Thomas, 1894
Hemitragus jemlahicus H. Smith, 1826
- Naemorhedus Hamilton Smith, 1827
Naemorhedus baileyi Pocock, 1914
Naemorhedus caudatus Milne-Edwards, 1867
Naemorhedus goral Hardwicke, 1825
Naemorhedus griseus Milne-Edwards, 1871
Naemorhedus caudatus Milne-Edwards, 1867
Naemorhedus goral Hardwicke, 1825
Naemorhedus griseus Milne-Edwards, 1871
- Oreamnos Rafinesque, 1817.
Oreamnos americanus Blainville, 1816
- Ovibos Blainville, 1816.
Ovibos moschatus Zimmermann, 1780
- Ovis Linnaeus, 1758
Ovis ammon Linnaeus, 1758
Ovis orientalis Linnaeus, 1758
Ovis canadensis Shaw, 1804
Ovis dalli Nelson, 1884
Ovis nivicola Eschscholtz, 1829
Ovis orientalis Linnaeus, 1758
Ovis canadensis Shaw, 1804
Ovis dalli Nelson, 1884
Ovis nivicola Eschscholtz, 1829
- Pseudois Hodgson, 1846
Pseudois nayaur Hodgson, 1833
Pseudois schaeferi Haltenorth, 1963
Pseudois schaeferi Haltenorth, 1963
- Rupicapra Blainville, 1816
Rupicapra pyrenaica Bonaparte, 1845
Rupicapra rupicapra Linnaeus, 1758
En el Género Ovis se incluye la oveja doméstica y diversas especies salvajes estrechamente relacionadas. Son cinco especies y numerosas subespecies, algunas de las cuales son consideradas en ocasiones como especies:
Rupicapra rupicapra Linnaeus, 1758
En el Género Ovis se incluye la oveja doméstica y diversas especies salvajes estrechamente relacionadas. Son cinco especies y numerosas subespecies, algunas de las cuales son consideradas en ocasiones como especies:
- Ovis ammon – argalí
- Ovis orientalis
- Ovis canadensis - carnero de las Rocosas.
- Ovis dalli - muflón de Dall
- Ovis nivicola - oveja de las nieves.
Existe un acuerdo general en la comunidad científica de que las ovejas salvajes (muflones) que habitan en Asia occidental son los antepasados de todas las razas de ovejas domésticas, Ovis aries (Groves y Grubb, 2011), siendo la misma especie según análisis de ADN, número de cromosomas o tipo de hemoglobina A. Sin embargo, hay cierto acuerdo entre los taxonomistas y zoólogos para nombrar estas formas silvestres de manera diferente como Ovis orientalis Gmelin, 1774 u Ovis gmelini Blyth, 1841, con más nombres diferentes subespecíficos. La denominación específica del muflón Europeo es bastante controvertida. Originalmente fue nombrado como Aegoceros musimon (Pallas, 1811). Algunas autoridades aún lo consideran como una especie completa (Ovis musimon), mientras que otros lo consideran una subespecie de argali (O. ammon musimon), de muflones asiáticos, (O. gmelini musimon u O. orientalis musimon) o de ovejas domésticas (O. aries musimon). Actualmente, la mayoría de los autores consideran que es una subespecie de muflones asiáticos u ovejas domésticas.
Es ampliamente reconocido que esta oveja se originó a partir de ovejas salvajes asiáticas que fueron traídas a Cerdeña por humanos alrededor de 8000 años aC, más tarde introducidas a Córcega y, probablemente, después de una fase de predomesticación, liberado en el medio silvestre 6000-7000 años aC. Dado que generalmente se supone que los muflones europeos son poblaciones salvajes de antiguas poblaciones nacionales, es recomendable denominarlos taxonómicamente como Ovis aries subespecie musimon siguiendo ITIS (2016). La oveja domestica según esta taxonomía sería Ovis aries aries, Linnaeus 1758.
Ovis aries musimon, Pallas 1811
El nombre de esta especie deriva todo del latín: "ovis" significa oveja, y "musimo, musmo, onis" significa muflón.
El género Ovis apareció en Asia en el periodo Plio-Pleistoceno hace 1,8 – 2,4 millones de años. Este taxón fue común en Asia y Este de Europa, pero era muy raro en el Centro y Oeste Europeo durante el Periodo Cuaternario. El muflón de Córcega se encontraba distribuido por todo el continente Europeo, hasta el periodo Neolítico. Los efectos de las glaciaciones, presión cinegética y posiblemente, la acción del hombre sobre su domesticación, redujeron su hábitat a Córcega, Cerdeña y Chipre y posiblemente a algunas regiones de Grecia. El primer proceso de domesticación de animales del género Ovis, posiblemente comenzó en regiones del Este de Europa durante el octavo milenio a.C. Este proceso de semidomesticación consistía en el mantenimiento de animales dentro de rediles con trolados con el objeto de aprovisionarse de recursos alimentarios (leche y carne), abrigo (pieles) y herramientas (huesos). Recientes estudios citogenéticos apoyan la hipótesis de que todos los muflones mediterráneos descienden de un primitivo ovino doméstico. El muflón de Córcega sería el resultado de la introducción durante el periodo Neolítico, 6.000-7.000 años a.C., de un muflón anatoliano (Ovis gmelini gmelini) semidomesticado que posteriormente retorna a su estado silvestre. Esta hipótesis ha sido confirmada mediante investigaciones paleontológicas y arqueológicas en Córcega y Chipre y mediante estudios genéticos en muflones de Cerdeña. Debido a la estrecha relación genética que presenta con la oveja, se considera al muflón como el más probable ancestro de la especie doméstica. A partir de las poblaciones originarias de las islas mediterráneas, el muflón comienza a introducirse en diferentes países del continente europeo a partir del siglo XVIII.
Los primeros ejemplares que se introdujeron en España lo fueron en la Serranía de Cuenca, en el Hosquillo, desde donde se llevaron a la Sierra de Cazorla en 1954. De estos núcleos, se han extendido por toda la Península, tanto en reservas de caza (como la de Puertos de Beceite, Muela de Cortes, etc.) como en cotos particulares y públicos de casi todas las provincias, llegando en los años 70 del pasado siglo al Parque Nacional del Teide. Actualmente se le encuentra por toda el área mediterránea de la Península Ibérica; se distribuye por los Puertos de Tortosa-Beceite, entre Tarragona, Teruel y Castellón, Tenerife (Parque nacional del Teide), Sierras Cazorla (Jaén) y Alcaraz (Albacete), la reserva de caza de la Muela de Cortes (Valencia), la sierra del Cid (Alicante), la Serranía de Cuenca, Serranía de Ronda (Málaga), el Parque Nacional de Cabañeros (Castilla La Mancha), Parque Natural de los Alcornocales (Cádiz), en el Pirineo Catalán, en la reserva de caza del Alt Pirineu (Lérida), en los montes do Invernadoiro (Orense) y en el Parque Natural de la Sierra de la Muela y Cabo Tiñoso en Cartagena (Región de Murcia). Sin embargo está ausente del Archipiélago Balear y de los territorios del norte de África. Debido a este potencial colonizador y constituir una amenaza grave para las especies autóctonas, los hábitats o los ecosistemas, esta especie ha sido incluida en el Catálogo Español de Especies exóticas Invasoras, aprobado por Real Decreto 630/2013, de 2 de agosto, restringido a las Islas Canarias.
Habita en espacios abiertos de montaña, generalmente accidentados, secos y duros que en el invierno no queden cubiertos de una gruesa capa de nieve.
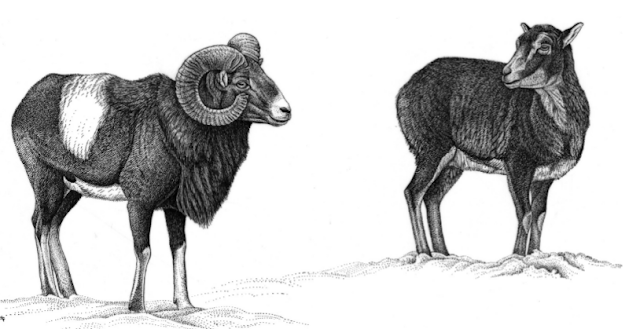
Son la forma más pequeña del género Ovis aunque el muflón europeo es un animal grande (longitud de cabeza y cuerpo de 127 a 145 cm, cola de 3,5 a 6 cm y altura a la cruz de 70-80cm) que puede pesar de 35-50 Kg los machos y 25-35 las hembras. Se asemeja a una oveja estilizada, de patas y cuello proporcionalmente más largos, con lana mucho más corta y de color pardo oscuro, volviéndose blanquecina en el morro, los ojos, la mitad inferior de las patas, los glúteos y el vientre.
El pelaje invernal es de color marrón chocolate con manchas blancas en las patas, la cara y la grupa, que es atravesada por una cola corta de color oscuro. El vientre es blanco. El pelaje de verano es mucho más claro que el de invierno y las manchas blancas casi desaparecen por completo.
El pelaje del muflón está constituido por dos tipos de pelo. El primero, denominado de cobertura, es largo, se origina en los folículos pilosos primarios de la piel y actúa como protección mecánica. De los folículos secundarios se origina el subpelo o vellón, más fino que el de cobertura, y que le confiere una protección térmica. La actividad folicular, así como la variación de la relación de folículos pilosos secundarios y primarios, está modulada por las variaciones anuales del fotoperiodo a través de la prolactina. La muda del pelo tiene lugar desde finales de mayo a principios de julio, con importantes variaciones individuales, observándose un retraso de la misma según aumenta la edad del animal. El comienzo del crecimiento del pelo (anagénesis) se produce alrededor
del solsticio de verano (finales de junio). Este crecimiento se mantiene constante hasta el solsticio de invierno (finales de diciembre), donde el pelo alcanza su máxima longitud (4-5 cm). El crecimiento del pelo está inversamente correlacionado con las variaciones anuales de secreción de prolactina. La disminución de las concentraciones plasmáticas de prolactina, desde el solsticio de verano al de invierno, coincide con el periodo de crecimiento del pelo, mientras que el incremento de sus niveles, en la primavera, actuarían como señal endocrina para el establecimiento de la muda.
Hay un claro dimorfismo sexual:
1) Son más grandes que las hembra
2) tienen unos cuernos grandes (máximo 80-90 cm) y curvados hacia atrás hasta casi cerrar un círculo, mientras que las hembras no presentan cuernos o los tienen muy pequeños (18 cm como máximo).
3) Tienen una gorguera de pelo en el cuello y el pecho y presentan una coloración general más oscura.
4) presentan una gran mancha blanca muy conspicua en medio de los flancos.
Básicamente diurno, en el invierno se le puede ver alimentarse desde el amanecer hasta la puesta del sol, mientras que en el verano muestra actividad sobre todo en las primeras horas de la mañana y la noche.
del solsticio de verano (finales de junio). Este crecimiento se mantiene constante hasta el solsticio de invierno (finales de diciembre), donde el pelo alcanza su máxima longitud (4-5 cm). El crecimiento del pelo está inversamente correlacionado con las variaciones anuales de secreción de prolactina. La disminución de las concentraciones plasmáticas de prolactina, desde el solsticio de verano al de invierno, coincide con el periodo de crecimiento del pelo, mientras que el incremento de sus niveles, en la primavera, actuarían como señal endocrina para el establecimiento de la muda.
Hay un claro dimorfismo sexual:
1) Son más grandes que las hembra
2) tienen unos cuernos grandes (máximo 80-90 cm) y curvados hacia atrás hasta casi cerrar un círculo, mientras que las hembras no presentan cuernos o los tienen muy pequeños (18 cm como máximo).
3) Tienen una gorguera de pelo en el cuello y el pecho y presentan una coloración general más oscura.
4) presentan una gran mancha blanca muy conspicua en medio de los flancos.
Básicamente diurno, en el invierno se le puede ver alimentarse desde el amanecer hasta la puesta del sol, mientras que en el verano muestra actividad sobre todo en las primeras horas de la mañana y la noche.
Vive en rebaños. En primavera y verano las hembras y los jóvenes forman en pequeños grupos familiares a los que se agrega un macho solamente en la época de celo. Los machos antes deben medir sus fuerzas con otros rivales, entrechocando sus cuernos violentamente.
La alimentación es puramente vegetariana, siendo posiblemente una de las especies de herbívoro que más especies diferentes consume por ingesta, llegándose a encontrar más de 100 variedades diferentes en un solo estómago. Consume indistintamente fanerógamas, criptógamas, hongos y líquenes, sin embargo, son las plantas herbáceas y las gramíneas, cuando están disponibles, las más apetecidas.
La alimentación es puramente vegetariana, siendo posiblemente una de las especies de herbívoro que más especies diferentes consume por ingesta, llegándose a encontrar más de 100 variedades diferentes en un solo estómago. Consume indistintamente fanerógamas, criptógamas, hongos y líquenes, sin embargo, son las plantas herbáceas y las gramíneas, cuando están disponibles, las más apetecidas.
Los machos son fértiles a partir de un año y medio de edad y pueden participar activamente en el proceso reproductivo a partir del tercer o cuarto año. Las hembras alcanzan la madurez con un año y medio, pariendo por primera vez a los dos años de edad. El período de celo se sitúa en el mes de noviembre en la mayoría de las poblaciones de la Península. El período de gestación dura alrededor de cinco meses. La mayoría de los partos acontece en marzo y abril, y habitualmente tienen una sola cría, considerándose las observaciones de hembras con dos crías como adopciones espontáneas y no como partos gemelares. Aunque no es frecuente, el muflón puede aparearse con ovejas domésticas (Ovis orientalis aries) descarriadas de tal manera que entre los rebaños de muflones podría observarse algún ejemplar con características intermedias.
Sus predadores mas peligrosos son lobos y osos. Los linces y águilas suelen depredar sobre los individuos más jóvenes.
Sus predadores mas peligrosos son lobos y osos. Los linces y águilas suelen depredar sobre los individuos más jóvenes.